Interictal epileptiform discharge(IED,发作间期癫痫样放电)不是一种单一波形,而是一组在发作间期出现、短暂、尖锐、突出于背景、常伴后随慢波的异常放电事件。临床上,IED 可以支持癫痫诊断、帮助综合征分类、提示 irritative zone 或 seizure-onset zone(SOZ)相关网络;但 IED 不能脱离病史和临床表现单独诊断癫痫,因为癫痫样异常也可偶见于无癫痫发作史人群 [3]。
最实用的理解方式是把 IED 放进四个维度:形态 morphology、空间分布 topography、时间组织 temporal organization、状态依赖 state relation。对 SEEG/iEEG 来说,还应再加一个维度:它与 SOZ、HFO、LoWS、传播方向和层状微环路之间的关系。
1. 定义边界:spike、sharp wave 与后随慢波
临床 EEG 术语中,spike 通常指 20 到小于 70 ms 的尖锐瞬变,sharp wave 指 70 到 200 ms 的尖锐瞬变;二者都应清楚区别于背景,并且常有后随慢波或背景扰动 [1]。这个 70 ms 分界主要是描述性约定,不应被理解为机制上的硬边界。
常见形态可以分成几类:
| 形态 | 核心特征 | 临床/分析注意点 |
|---|---|---|
| Spike | 20 到小于 70 ms,尖锐、短暂 | 需要区别肌电、电极噪声和正常尖波变异 |
| Sharp wave | 70-200 ms,较宽但仍尖锐 | 临床意义通常与 spike 类似 |
| Spike-and-slow-wave | spike 后接慢波 | 可局灶,也可广泛性;慢波使复合波更显眼 |
| Sharp-and-slow-wave | sharp wave 后接慢波 | 常见于局灶性癫痫样放电报告 |
| Polyspike | 两个或更多 spike 连续出现 | ACNS 将 polyspike 描述为无明显 interdischarge interval、总时长小于 0.5 s 的连续 spike [2] |
| Polyspike-and-wave | 一串 spike 后接慢波 | 常见于广泛性癫痫谱系,也可局灶出现 |
| Periodic discharges | 形态近似的放电按相对固定间隔反复出现 | 属于 rhythmic/periodic patterns,不等同普通散发 IED |
| BIRDs | 短阵、节律性、潜在发作样放电 | ACNS 定义为大于 4 Hz、0.5 到小于 10 s、非正常变异、无明确临床相关并满足特定特征的 rhythmic activity [2] |
因此,判断一个事件是不是 IED,不能只看“尖不尖”。还要看它是否突出于背景、是否有合理电场分布、是否伴随后随慢波或背景扰动、是否符合该年龄和状态下的正常变异,以及是否可以被伪迹解释。
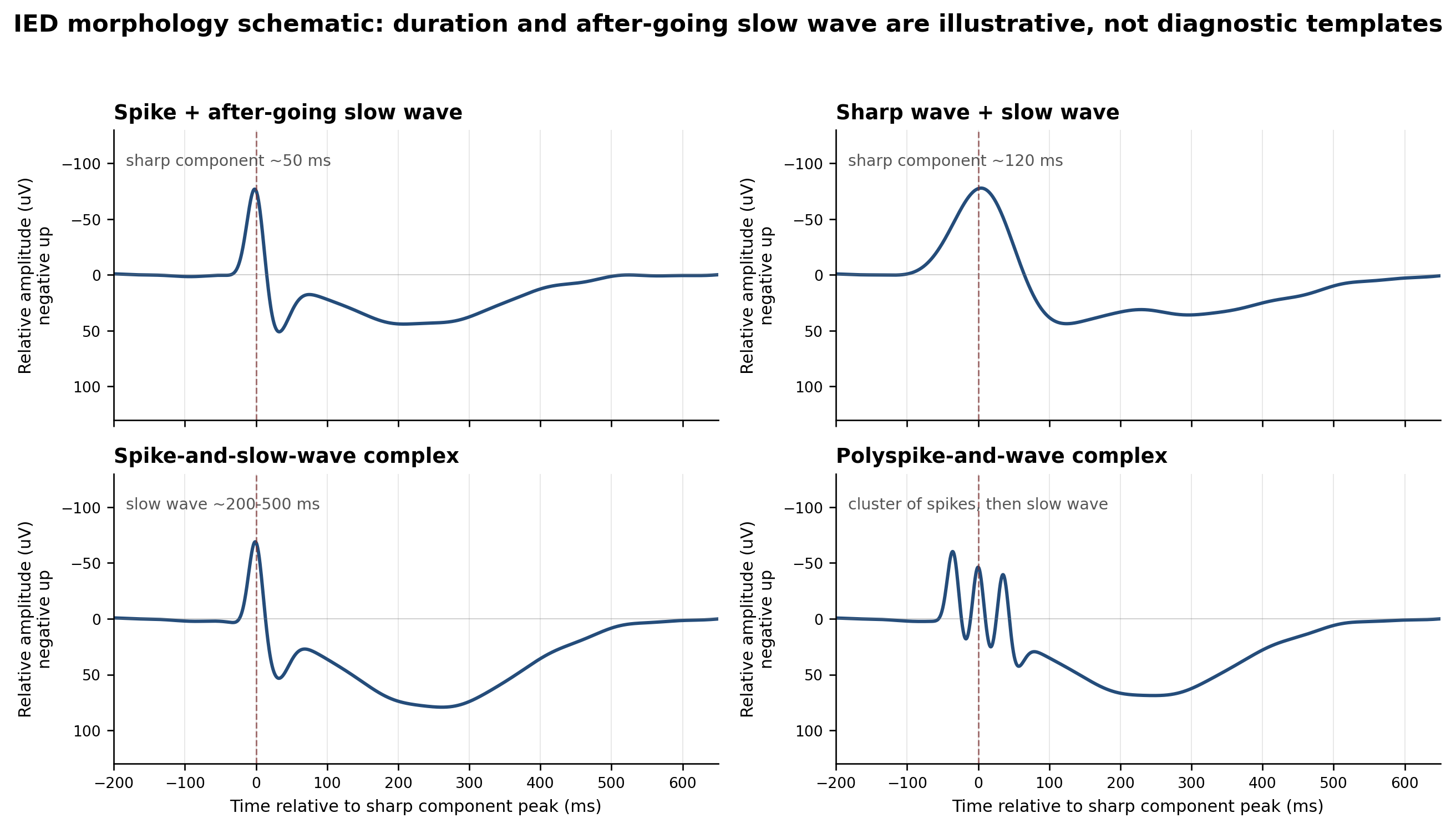
图 1. IED 形态教学示意图。该图为原创示意,不是患者数据,也不是从单篇论文直接截图;目的是把 spike、sharp wave、spike-and-slow-wave 和 polyspike-and-wave 的时间尺度与后随慢波关系画清楚。真实判读不能只套图形模板,还要结合电场、背景、状态、伪迹和临床上下文。
2. 空间分布:同样的波形,定位意义完全不同
IED 的临床意义高度依赖空间分布。一个 left anterior temporal sharp wave 与 generalized spike-and-wave 的诊断方向完全不同。常用描述包括 focal、regional、multifocal、generalized、lateralized、bilateral independent、unilateral independent 和 multifocal periodic。
ACNS 2021 术语体系把 critical care EEG 中 rhythmic/periodic patterns 的空间主项系统化为 generalized、lateralized、bilateral independent、unilateral independent、multifocal 等,并强调这些术语服务于标准化报告和多中心研究 [2]。
在 SEEG/iEEG 中,空间分布还需要更细:不仅要报告“哪个脑叶”,还要描述 contacts、极性反转、局部场域、是否跨电极传播、是否只在某个接触点最大、是否与病灶/切除区/SOZ 重叠。宏观 scalp EEG 的 generalized 或 regional pattern,在 SEEG 里可能拆成多个局灶起源和传播通路。
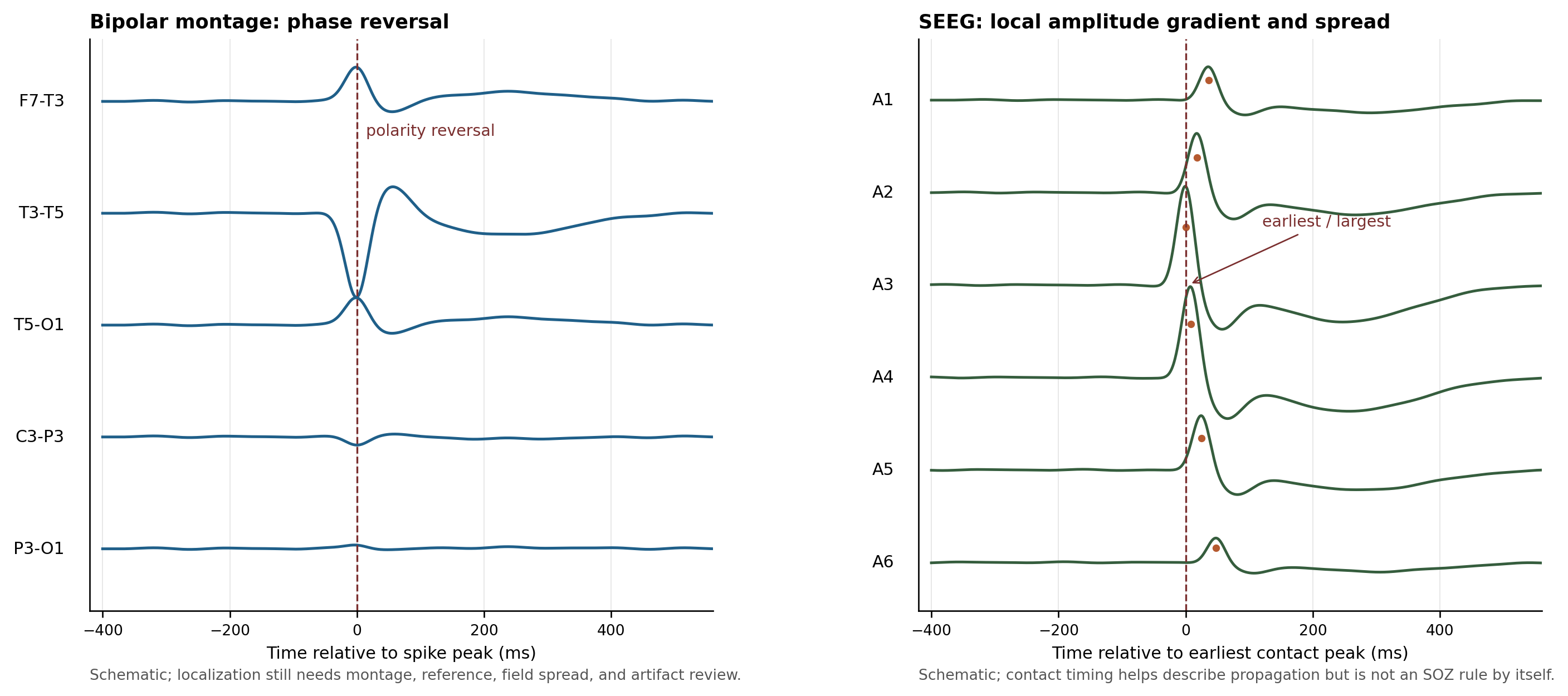
图 2. 空间组织教学示意图。左侧展示双极导联中相位反转对局部场最大点的提示作用;右侧展示 SEEG contact 层面可能出现的毫秒级传播和幅度梯度。该图同样为原创示意,不代表真实患者定位结论;SOZ 判断仍需结合发作起始、影像、半定量频率、HFO/LoWS、刺激反应和术后结局等证据。
3. 时间组织:从散发 IED 到 ictal-interictal continuum
IED 的时间组织可以看成一条连续谱:
sporadic spike/sharp |
ACNS 2021 对 electrographic seizure 给出实用门槛:epileptiform discharges 平均频率大于 2.5 Hz 且持续至少 10 s,或任意有明确演变并持续至少 10 s 的 EEG pattern,可归入 electrographic seizure;而 BIRDs 覆盖的是大于 4 Hz、0.5 到小于 10 s 的短阵潜在发作样 rhythmic activity [2]。
这条边界对读图很重要:尖锐不等于发作,周期性也不等于发作。需要同时判断频率、持续时间、演变、临床相关性、背景状态和治疗反应。对 SEEG 分析来说,尤其不能把所有高频短阵或周期性 sharp activity 直接归为 seizure onset;它们可能位于 ictal-interictal continuum,也可能只是 irritative network 的一部分。
4. 状态依赖:睡眠、慢波和 IED 表达
IED 的出现率具有强状态依赖。NREM 睡眠常增强癫痫样活动,但这种增强不是简单的“睡眠状态效应”,而可能与慢波周期中的特定相位有关。Frauscher 等在同步 scalp-intracerebral EEG 中分析 8 名药物难治性局灶癫痫患者,发现 79% 的 spikes 和 65% 的 HFOs 出现在高波幅广泛慢波期间,spike/HFO 密度在从 up-state 到 down-state 的转换附近最高 [5]。
这提示 IED 更容易被同步化窗口组织,而不仅是由兴奋性升高触发。对临床报告来说,应该明确 IED 是否 sleep-activated、是否只在 NREM 出现、是否与慢波相位耦合、REM 中是否消失或减少。对自动检测来说,状态依赖也意味着模型不能只学局部波形,还应纳入睡眠分期、背景节律和慢波相位等上下文。
5. IED 与 HFO、LoWS、SOZ:相关但不能混同
IED、HFO、LoWS 和 SOZ 是不同层级的概念。
IED 是低频段可见的尖/棘/尖慢波事件。HFO 通常指 80-500 Hz 范围的 high-frequency oscillations,可分为 ripple 和 fast ripple,是癫痫灶定位研究中的重要候选 biomarker;HFO 常与 IED 共现,但也可以独立于 spike 出现,因此不能把 HFO 简化为 IED 的高频成分 [7]。
LoWS 是 local wake slow waves,反映清醒状态下局部慢波/局部睡眠样活动。近期研究提示 LoWS 与 IED 可发生时间聚集,并且 LoWS 变化可能提供不同于 IED rate 的 EZ/SOZ 信息 [8]。因此,在分析 pipeline 中应避免把 IED 后随慢波误当成独立 LoWS,也要避免把 LoWS 的局部慢相位误判为 epileptiform discharge。
SOZ 是发作起始区。IED rate、IED density、spike burst、HFO、IED-HFO coupling、IED propagation、phase-amplitude coupling、connectivity 和 LoWS 都可能提供 SOZ 线索,但都不是单独金标准。Smith 等在人类 microelectrode array 记录中发现多数 IED 呈 traveling waves,并且传播路径与 ictal discharges 有相似性,提示 IED 的传播方向本身也可携带定位信息 [6]。
Silva 等 2026 年的 Neuropixels 研究进一步把 IED 推进到层状细胞微环路尺度:他们在癫痫手术患者新皮层 epileptogenic tissue 中记录 1,152 个神经元和 1,094 个 IED,发现 IED 周围神经元 firing 并非简单同步爆发,而是由 early activation、suppression、late activation 等不同相位群体组成;表层 regular-spiking cells 参与 sharp discharge 幅度编码,E/I imbalance 可在 IED 前最高约 1,000 ms 预示事件形成 [4]。这说明 IED 不只是宏观波形,也是一个可预测的层状-细胞状态转移。
6. IED 自动检测方法综述
IED 自动检测的目标不是替代医生“判读整份 EEG”,而是在长时程 EEG/SEEG 中高效、可复现地定位候选事件,并为统计分析、SOZ 定位、闭环刺激或大规模队列研究提供事件层数据。一个成熟检测系统通常包括六步:
信号预处理 |
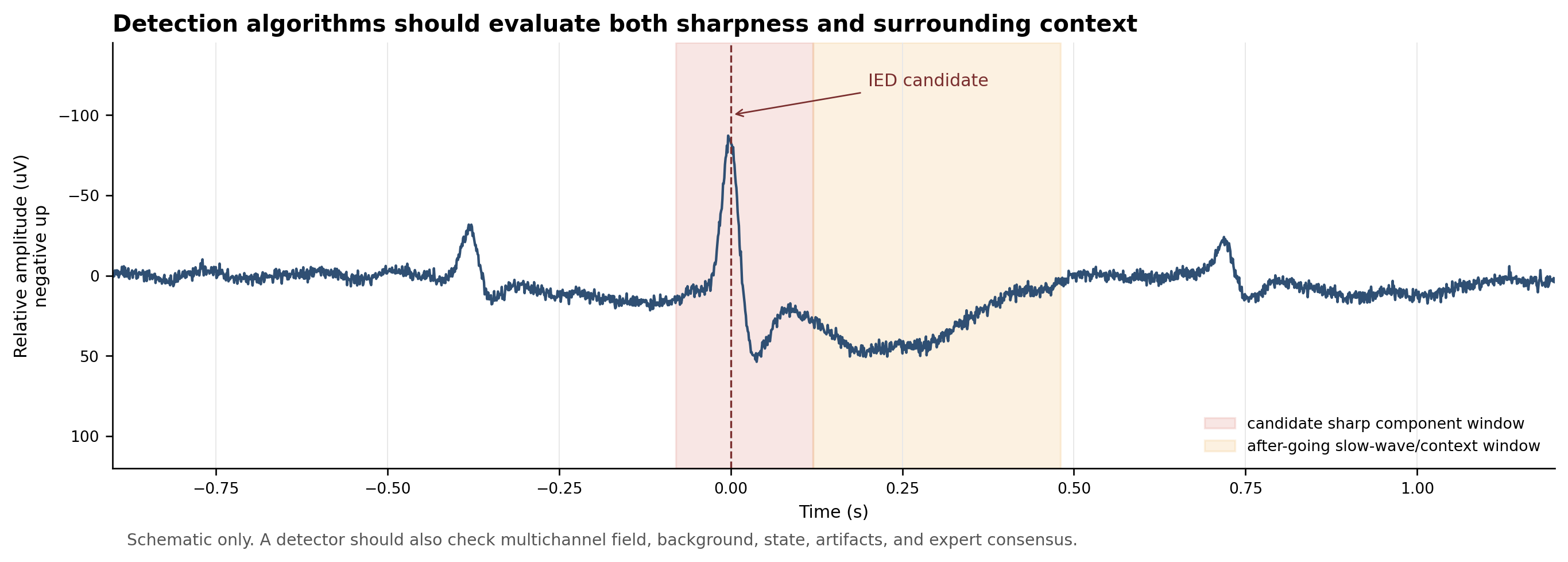
图 3. IED 检测窗口教学示意图。候选事件不应只看瞬时尖锐成分,还要检查后随慢波、背景扰动、相邻通道场分布和前后状态。该图为合成波形,用于解释检测逻辑,不是模型训练样本或诊断标准。
6.1 人工视觉判读仍是参照标准,但不是完美 gold standard
IED 识别本身有主观阈值。JAMA Neurology 的多中心研究曾让 8 名 fellowship-trained clinical neurophysiologists 标注 13,262 个候选 IED,结果显示专家对“整份 EEG 是否含 IED”的一致性较好,但对单个事件的判定一致性较低,差异很大程度来自不同专家使用了不同判断阈值 [15]。
这对算法评价很关键:如果训练标签来自单一专家,模型会学习该专家的阈值;如果标签来自多专家共识,模型可能更稳健,但会牺牲一些边界事件。实际应用中,应区分 event-level detection、record-level classification 和 localization-level inference。一个模型 event-level false positive 较多,不一定不能作为预筛工具;但如果用于闭环刺激或 SOZ 定位,误报成本就高得多。
6.2 规则/拟人化 mimetic 方法
早期自动检测尝试把 EEG 医生的视觉规则写成算法:寻找短时高斜率、高尖锐度、相对背景突出的瞬变,再检查持续时间、幅度、后随慢波和局部场域。这类方法可解释性强,容易和 spike/sharp wave 的定义对齐。
主要缺点是上下文不足。IED 与伪迹、vertex sharp transient、lambda wave、breach rhythm、triphasic waves、RDA+S 等模式在局部形态上可能相似;单靠 duration、amplitude、sharpness 很容易误报。Handbook of Clinical Neurophysiology 对自动 IED 检测的综述早已指出:计算机可以编码幅度、时长、尖锐度等局部规则,但经验丰富的 EEG 医生还会综合状态、年龄、电场、背景、空间传播和伪迹线索 [13]。
6.3 模板匹配与人机协同
模板匹配的基本思路是:由专家或已有数据库提供典型 IED 模板,在新记录中寻找与模板高度相似的片段。它适合病人内、形态相对固定的 spike,也适合 SEEG 中重复出现的局部 sharp event。
Lodder 与 van Putten 的 self-adapting system 使用大量模板生成候选 IED,再按置信度排序给医生复核,并可根据复核反馈自适应更新 [12]。SpikeGUI 则将模板匹配与 online machine learning 结合,用于加速专家标注 interictal discharges [14]。
模板方法的优势是低样本、可交互、易部署;弱点是跨患者泛化差,对形态变化、状态变化、参考导联变化和伪迹敏感。SEEG 中如果某个 contact 的 IED 形态稳定,模板匹配很实用;但如果目标是跨患者通用检测,模板库必须足够大,并需要持续复核和校准。
6.4 特征工程:时域、频域、时频与非线性特征
传统机器学习通常先提取特征,再用 SVM、random forest、logistic regression、LDA 等分类器判断候选事件。常见特征包括:
| 特征类别 | 示例 | 对 IED 的意义 |
|---|---|---|
| 时域形态 | peak amplitude、duration、slope、sharpness、area | 对应 spike/sharp wave 的视觉定义 |
| 背景对比 | event/background amplitude ratio、local z-score | 区分突出事件与普通背景波 |
| 空间电场 | channel spread、phase reversal、bipolar polarity | 区分真实脑源事件和伪迹 |
| 频域/时频 | wavelet coefficients、短时能量、spectrogram | 捕捉尖波的宽频瞬变和 HFO 共现 |
| 非线性特征 | entropy、fractal dimension、复杂度指标 | 描述局部动态变化 |
| 上下文特征 | sleep stage、state transition、slow-wave phase | 处理状态依赖和误报 |
2024 年 Comput Biol Med 综述把 IED 检测方法归为六类:template matching、feature representation、matrix decomposition、tensor factorization、neural networks,以及 scEEG-to-iEEG estimation 后检测分类 [9]。这个分类很适合组织方法学综述:从手工特征到表征学习,从单通道波形到多通道矩阵/张量结构,再到 scalp 与 intracranial 之间的信息转换。
6.5 矩阵分解和张量方法
IED 不是单通道事件,而是多通道时空模式。矩阵分解和张量方法试图利用 channel × time × frequency × trial 的结构,把重复出现的空间场和时间波形分离出来。
这类方法特别适合 SEEG/iEEG:IED 可能在多个 contacts 中以固定时延传播,也可能在某些频段上伴随 HFO 或 high-gamma burst。矩阵/张量分解可以把“共同模式”从噪声和伪迹中拆出来,辅助发现 propagation cluster、dominant spatial field 或 patient-specific IED subtype。
局限是解释门槛较高,且分解出的成分未必天然等于生理事件。通常需要与人工标注、SOZ、影像病灶、手术切除范围和预后一起验证。
6.6 深度学习:从 scalp EEG 到 iEEG/SEEG
深度学习的优势是直接从波形、时频图或多通道片段中学习特征,减少手工规则。Jing 等开发的 SpikeNet 使用 9,571 份 scalp EEG 训练 deep neural network,测试集来自 13,262 个由 8 名专家标注的 IED candidates,并构建了整份 EEG 的 IED-positive/negative 分类器;该研究报告 SpikeNet 在校准误差和 AUC 等指标上达到或超过专家和商业检测器 [10]。
iEEG/SEEG 方面,Geng 等提出 IEDnet,使用 LSTM/RNN 架构并结合 AC-GAN 数据增强,在两个真实 iEEG 数据集上验证,对采样率和噪声具有一定鲁棒性,并展示跨机构泛化能力 [11]。AiED 则将模板匹配与 CNN 结合,用 spectrogram 训练 intracranial IED 分类器,在 307 名难治性癫痫患者的 intracranial EEG 样本上进行专家标注和验证 [16]。
深度学习方法的主要挑战包括:标注成本高、标签不一致、跨中心导联/采样率/滤波差异、伪迹和 breach effect、不同病因导致的形态漂移、可解释性不足,以及事件级高性能不一定能转化为可靠的 SOZ 定位。最稳妥的落地方式不是“全自动替代医生”,而是“高召回候选生成 + 置信度排序 + 人工复核 + 可审计统计”。
6.7 SEEG/iEEG 检测的特殊问题
SEEG 与 scalp EEG 相比,信噪比和空间分辨率更高,但也带来新的检测问题。
第一,SEEG 的 IED 可以非常局灶,只出现在一两个 contacts;如果算法要求广泛空间场,可能漏检。第二,SEEG 中生理 high-gamma、HFO、肌电、导线噪声、电刺激残留和接触不良都可生成尖锐瞬变。第三,同一患者不同 contacts 的背景差异很大,统一阈值容易失败。第四,IED 的传播方向、延迟和相位反转有定位意义,后处理不能只保留单个 peak time。
一个面向 SEEG 的 IED 检测 pipeline 应至少包括:
- 分 contact 的噪声和坏道标记。
- 统一重参考策略,如 bipolar、common average 或局部参考,并记录参考方式。
- 候选事件生成,使用高召回策略保留 spike、sharp、spike-wave、polyspike 候选。
- 多通道合并,把同一事件在邻近 contacts 的表现合成一个 event object。
- 事件属性计算,包括 peak time、duration、sharpness、polarity、field size、phase reversal、after-going slow wave、HFO co-occurrence、state、SOZ/resection overlap。
- 分类器或规则分层,区分 definite IED、probable IED、artifact/benign variant、periodic/rhythmic pattern、BIRDs/seizure-like run。
- 人工复核界面,按置信度、区域、睡眠状态、事件簇或疑似 SOZ 排序。
- 输出事件表和统计表,而不是只输出一串时间点。
6.8 评价指标:不要只报 accuracy
IED detection 的评价必须按用途区分。
| 用途 | 重点指标 | 原因 |
|---|---|---|
| 快速预筛 | sensitivity、false positives/hour | 漏检比误报更严重,但误报不能淹没医生 |
| 研究统计 | event-level precision/recall、temporal tolerance | 事件时间点和数量会影响后续分析 |
| 记录级诊断辅助 | EEG-level AUC、calibration、specificity | 关心整份 EEG 是否含 IED |
| SOZ/IZ 定位 | channel-level rate、density、spatial concordance、outcome association | 事件检测只是定位链条的一环 |
| 闭环刺激 | latency、online performance、false stimulation rate | 实时性和安全性比离线 AUC 更关键 |
Accuracy 在 IED 检测中常常误导,因为长时程 EEG 里负样本远多于正样本。一个几乎不报 IED 的模型也可能有高 accuracy,但没有临床价值。更合理的是同时报告 sensitivity、specificity、precision、false positives/hour、calibration、event-level F1、record-level AUC,并说明 temporal matching window 和 expert consensus 标准。
7. 实战描述:一条 IED 报告应包含什么
临床或研究中描述 IED,不应只写“有 spike”。更完整的句式是:
某部位 + 某形态 + 某频度 + 某状态下增强 |
例如:
Frequent left anterior temporal sharp-and-slow-wave discharges, |
SEEG 中可以进一步写成:
Frequent sharp-and-slow-wave discharges maximal at LAMY3-4 and LHIP1-2, |
这种描述把形态、定位、状态、时间组织和伴随特征都保留下来,后续才能和 SOZ、影像、认知任务、切除范围和预后做系统关联。
8. 容易误判为 IED 的模式
| 混淆项 | 为什么像 IED | 避免误判的关键 |
|---|---|---|
| Benign variants | 可有尖锐形态 | 看年龄、状态、典型分布、是否有后随慢波和背景扰动 |
| Artifact | 肌电、眼动、电极噪声可很尖 | 看空间同步性、生理电场、是否跨导联不合理 |
| Breach rhythm | 颅骨缺损处高波幅、尖锐、快频 | 结合手术史、颅骨缺损位置和持续背景特征 |
| Triphasic waves | 三相 sharp-like morphology | 多见代谢/结构性脑病,常弥漫、双额优势 |
| RDA/LRDA | 节律性 delta 可 sharply contoured | 需看是否有 plus modifier、演变、频率和临床相关 |
| Post-IED slow wave | IED 后慢波可能被当成独立慢波 | 看是否紧跟 spike/sharp;LoWS 分析应排除 IED 后窗口 |
| Physiological HFO | SEEG 中生理高频活动很常见 | 结合区域、睡眠状态、IED 关系、SOZ 和慢波相位 |
9. 小结
IED 的核心不在“尖波清单”,而在四维组织:形态、空间、时间、状态。形态告诉我们它像什么,空间告诉我们它从哪里来,时间组织告诉我们它离 ictal pattern 多近,状态依赖告诉我们它在什么网络条件下容易出现。SEEG/iEEG 进一步要求把 IED 放入 HFO、LoWS、传播路径、SOZ 和层状微环路中理解。
自动检测方法的发展从规则和模板匹配,走到特征工程、矩阵/张量分解和深度学习。现在的趋势不是简单追求一个全自动 detector,而是建立可复核、可解释、可跨中心校准的检测-统计-定位 pipeline。对临床和研究最有价值的输出,也不是“检测到多少个 spike”,而是每个事件的形态、位置、状态、传播、伴随 HFO/慢波、置信度和与 SOZ/切除区的关系。
文献边界
本文以 seeg/IED 中的 Silva 2026 作为 IED 微环路核心文献,并补充了术语标准、睡眠/慢波调制、HFO/LoWS 关系和自动检测方法文献。当前材料对儿童癫痫综合征、neonatal EEG、药物诱发/代谢性 periodic patterns、以及商用软件横向评测覆盖有限;若后续作为正式综述,可继续扩展这些方向。
参考文献
[1] Kane N, Acharya J, Beniczky S, et al. A revised glossary of terms most commonly used by clinical electroencephalographers and updated proposal for the report format of the EEG findings. Revision 2017. Clinical Neurophysiology Practice. 2017;2:170-185. https://pubmed.ncbi.nlm.nih.gov/30214992/
[2] Hirsch LJ, Fong MWK, Leitinger M, et al. American Clinical Neurophysiology Society’s Standardized Critical Care EEG Terminology: 2021 Version. Journal of Clinical Neurophysiology. 2021;38(1):1-29. https://www.acns.org/UserFiles/file/ACNSStandardizedCriticalCareEEGTerminology_rev2021.pdf
[3] Aschner A, Kowal C, Arski O, et al. Prevalence of epileptiform electroencephalographic abnormalities in people without a history of seizures: A systematic review and meta-analysis. Epilepsia. 2024;65(3):583-599. https://pubmed.ncbi.nlm.nih.gov/38101821/
[4] Silva AB, Marathe SA, Greicius QR, et al. Laminar organization of cellular microcircuits modulating human interictal epileptiform discharges. Nature Neuroscience. 2026. https://doi.org/10.1038/s41593-026-02258-4
[5] Frauscher B, von Ellenrieder N, Ferrari-Marinho T, Avoli M, Dubeau F, Gotman J. Facilitation of epileptic activity during sleep is mediated by high amplitude slow waves. Brain. 2015;138(6):1629-1641. https://academic.oup.com/brain/article/138/6/1629/2847386
[6] Smith EH, Liou JY, Merricks EM, et al. Human interictal epileptiform discharges are bidirectional traveling waves echoing ictal discharges. eLife. 2022;11:e73541. https://pubmed.ncbi.nlm.nih.gov/35050851/
[7] Urrestarazu E, Chander R, Dubeau F, Gotman J. Interictal high-frequency oscillations (100-500 Hz) in the intracerebral EEG of epileptic patients. Brain. 2007;130(9):2354-2366. https://academic.oup.com/brain/article/130/9/2354/289977
[8] Sheybani L, Vivekananda U, Sinha N, et al. Dynamic Interplay Between Wake Slow Waves and Epileptiform Discharges in the Epileptogenic Zone. Neurology. 2025. https://pubmed.ncbi.nlm.nih.gov/40834347/
[9] Abdi-Sargezeh B, Shirani S, Sanei S, et al. A review of signal processing and machine learning techniques for interictal epileptiform discharge detection. Computers in Biology and Medicine. 2024;168:107782. https://pubmed.ncbi.nlm.nih.gov/38070202/
[10] Jing J, Sun H, Kim JA, et al. Development of Expert-Level Automated Detection of Epileptiform Discharges During Electroencephalogram Interpretation. JAMA Neurology. 2020;77(1):103-108. https://jamanetwork.com/journals/jamaneurology/article-abstract/2752666
[11] Geng D, Alkhachroum A, Bicchi MAM, et al. Deep learning for robust detection of interictal epileptiform discharges. Journal of Neural Engineering. 2021;18(5). https://pubmed.ncbi.nlm.nih.gov/33770777/
[12] Lodder SS, van Putten MJAM. A Self-Adapting System for the Automated Detection of Inter-Ictal Epileptiform Discharges. PLOS ONE. 2014;9(1):e85180. https://pmc.ncbi.nlm.nih.gov/articles/PMC3893182/
[13] Burgess RC, Turnbull JP. Automatic detection of interictal epileptiform discharges. In: Handbook of Clinical Neurophysiology. Elsevier; 2003:73-84. https://www.sciencedirect.com/science/article/abs/pii/S1567423103030065
[14] Jin J, Dauwels J, Cash SS, Westover MB. SpikeGUI: software for rapid interictal discharge annotation via template matching and online machine learning. Annual International Conference of the IEEE Engineering in Medicine and Biology Society. 2014;2014:4435-4438. https://pmc.ncbi.nlm.nih.gov/articles/PMC4416962/
[15] Jing J, Herlopian A, Karakis I, et al. Interrater Reliability of Experts in Identifying Interictal Epileptiform Discharges in Electroencephalograms. JAMA Neurology. 2020;77(1):49-57. https://pmc.ncbi.nlm.nih.gov/articles/PMC6806666/
[16] Quon RJ, Meisenhelter S, Camp EJ, et al. AiED: Artificial intelligence for the detection of intracranial interictal epileptiform discharges. Clinical Neurophysiology. 2022;133:1-8. https://pubmed.ncbi.nlm.nih.gov/34773796/