脑组织通常被描述为高度依赖葡萄糖的器官,但这句话容易遮住一个更细的问题:突触活动真正发生在轴突末梢、树突棘和局部微回路里,能量需求既快又局部。如果只从全脑供能或血糖水平理解神经元代谢,就会漏掉“局部燃料储备”和“局部调制输入”这两个层面。Kumar 等关于神经元甘油三酯和脂滴的研究,把脂滴从病理堆积物重新放回突触能量供应的框架中 [1];Meli 等关于 focal cortical dysplasia type 2b 的研究,则显示 FCD 病灶不只是皮层层化异常和畸形神经元,还伴随多巴胺轴突输入和受体表达的结构性改变 [2]。
这两篇文章研究对象不同:一篇问神经元能不能持续利用脂滴中的脂肪酸,一篇问 FCD type 2b 病灶里的多巴胺调制系统是否异常。把它们放在一起读,重点不是说 FCD 是一种脂质代谢疾病,而是提醒我们:局灶性癫痫病灶可能同时涉及结构发育、能量供应、轴突输入、受体表达和活动状态之间的耦合。病灶不是静态疤痕,而是一个持续运行、持续消耗、持续被调制的局部网络。
1. 脂滴不是静止仓库,而可能是突触活动的局部燃料池
传统观点里,健康神经元很少能看到大量 lipid droplets,因此“神经元不靠脂肪酸氧化供能”很容易成为默认假设。Kumar 等的贡献在于把这个推理倒过来:脂滴少,不一定说明神经元不用脂滴;也可能说明脂滴处在快速周转状态,生成后很快被动员 [1]。
这篇研究围绕 DDHD2 展开。DDHD2 是神经元相关的 triglyceride lipase,也是复杂型 hereditary spastic paraplegia 的相关基因。作者观察到,阻断 DDHD2 或阻断 mitochondrial lipid transporter CPT1 后,成年雄性小鼠会快速进入 torpor-like 状态;在体外神经元中,抑制 DDHD2 或降低电活动会导致脂滴积累,且脂滴可以出现在轴突和 nerve terminals。更关键的是,脂滴来源的脂肪酸会以活动依赖的方式进入线粒体,并支持局部 mitochondrial ATP production [1]。
这里的逻辑链很重要。第一,DDHD2 不只是一个“清除脂滴”的酶,它更像脂滴燃料流的出口。第二,脂滴积累不一定是单纯有害堆积,也可能说明燃料动员通路被堵住。第三,神经活动本身调节脂滴使用:沉默神经元会增加脂滴,而活动时脂肪酸更需要进入线粒体。也就是说,脂滴、脂肪酸氧化和突触活动之间不是并列关系,而可能构成一个局部能量闭环。
这个发现对癫痫研究有潜在意义。癫痫网络的核心特征之一是异常高频、同步和反复的放电。任何能影响轴突末梢 ATP 供应、囊泡循环、离子泵恢复和线粒体负荷的机制,都可能改变网络兴奋性阈值。脂滴燃料通路不一定直接“导致发作”,但它可能影响神经元在高负荷活动下如何维持、失败或转入异常状态。
2. FCD type 2b 不是单纯结构病灶,还改变多巴胺调制地形
FCD type 2 是药物难治性局灶性癫痫的重要病理基础,典型特征包括皮层层化异常、dysmorphic neurons 和 balloon cells。过去对 FCD 的理解常集中在 mTOR 信号、皮层发育、细胞形态和局部兴奋性上。Meli 等把问题推进到另一个层面:如果 FCD 常位于额叶,而额叶皮层又高度依赖来自脑干的 monoaminergic projections,那么病灶中的多巴胺轴突输入和多巴胺受体表达是否也被重塑 [2]?
作者使用两条路线互相印证。一条是在小鼠 medial prefrontal cortex 中建立 p.Leu2427Pro mTOR hyperactivation 模型,模拟 FCD type 2 相关的皮层发育异常;另一条是分析人类 FCD type 2b 手术标本,比较同一患者组织中的 control area 和 FCDIIB area。小鼠模型中,突变 mTOR 细胞表现出迁移异常、细胞体增大和 mTOR 通路活化;在人类标本中,作者结合 NeuN、SMI32、TH 轴突追踪和 DRD1/DRD2 RNA 原位杂交,直接观察病灶区的多巴胺输入与受体表达。
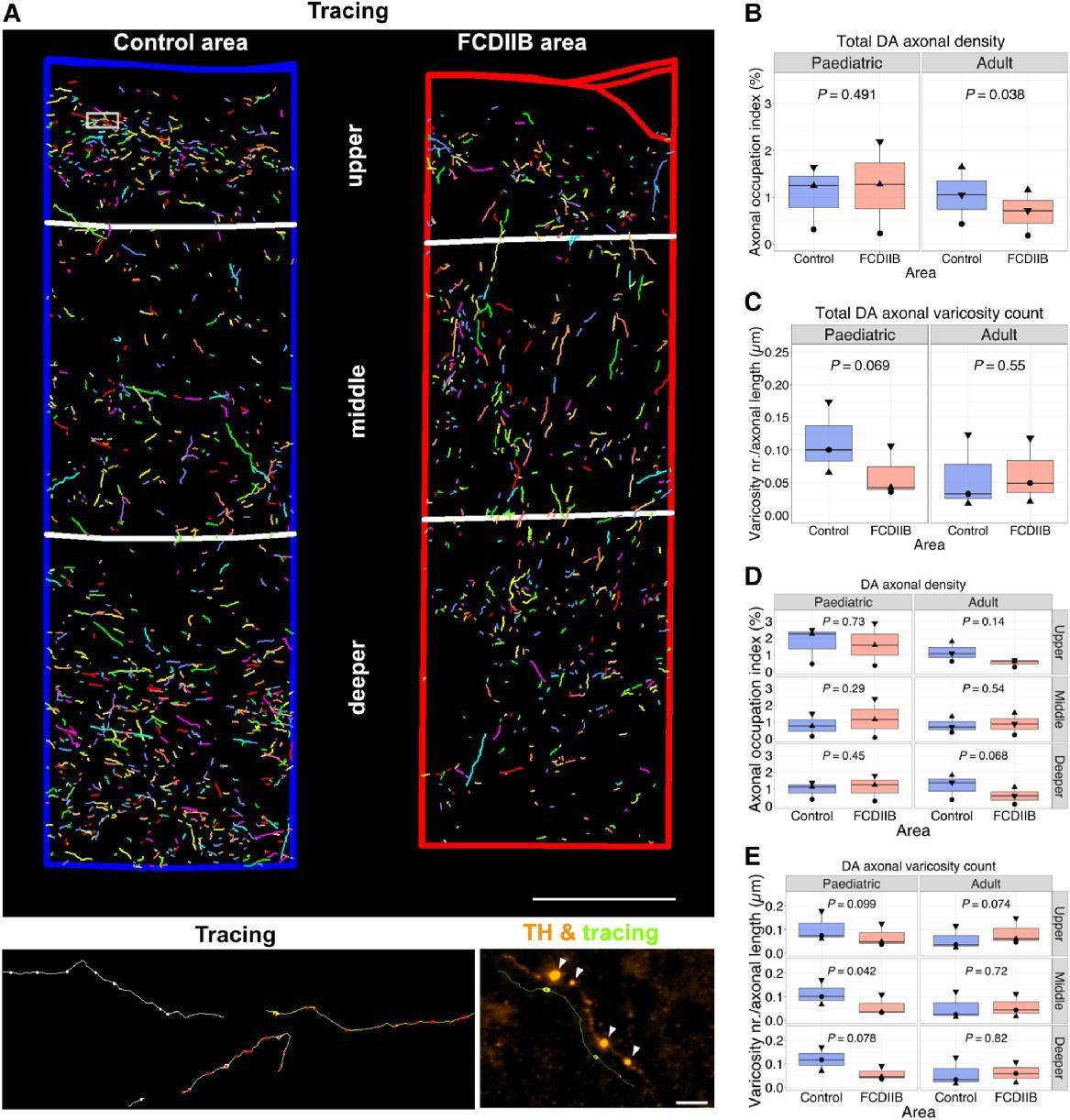
图 1. Meli 等 2025 原文 Figure 4,展示人类 FCD type 2b 区域中 dopaminergic axons 的三维追踪、总轴突密度、varicosity density 以及分层统计 [2]。原文为 CC BY 4.0 开放获取。
图 1 说明。 左侧的 A 部分把 control area 和 FCDIIB area 中的 TH-positive axons 做三维追踪,并按 upper、middle、deeper layers 分层。右侧 B-E 分别量化 total DA axonal density、varicosity count,以及不同层中的轴突密度和 varicosity count。最值得注意的是 adult specimens:FCDIIB area 的总体 DA axonal density 相比 control area 显著下降,且原本较有层化特征的多巴胺轴突分布被打乱。儿童标本中,总轴突密度变化不明显,但 varicosity count 在部分层面下降,提示发育阶段可能影响“轴突数量”和“释放位点样结构”的表现形式。
这张图的意义不在于单一统计显著性,而在于它把 FCD 病灶从“细胞形态异常”扩展为“调制输入地形异常”。多巴胺轴突不是均匀背景噪声,它携带与动机、注意、兴奋性调节、突触可塑性和发育成熟相关的信号。若 FCDIIB 区域的 DA 输入减少或层化模式改变,那么同一局部电路接收到的调制权重就会不同,进而可能影响发作阈值、发作传播和病灶周围网络的可塑性。
3. 受体表达升高说明病灶细胞并非只是“被输入减少”
如果只看到 DA axonal density 下降,容易得出一个过度简单的结论:FCD 病灶就是多巴胺输入不足。Meli 等进一步检测 DRD1 和 DRD2 mRNA,结果提示事情更复杂。无论在小鼠 mTOR-mutant neurons 还是在人类 FCD type 2b dysmorphic neurons 中,多巴胺受体表达都有上调趋势或显著上调 [2]。
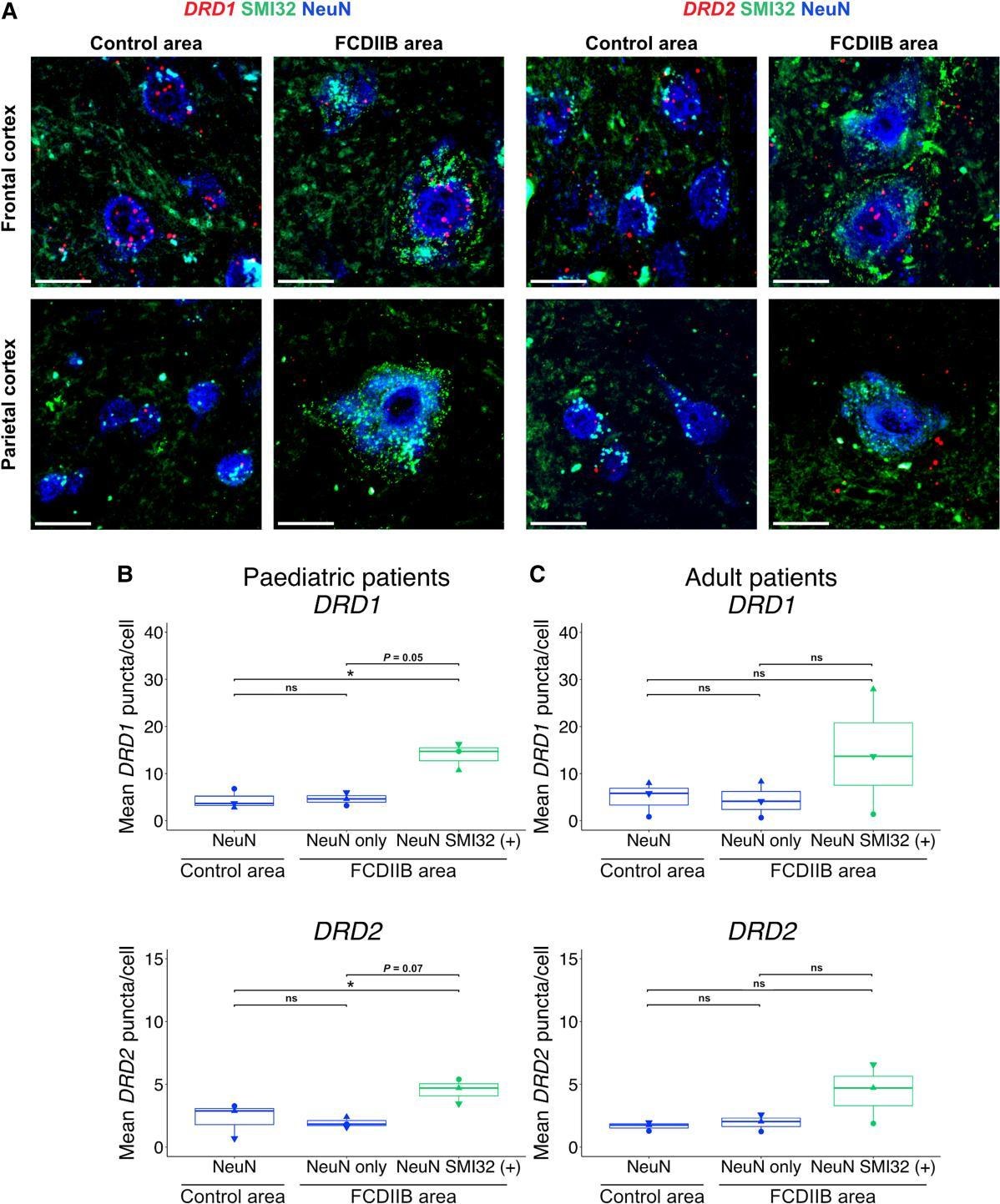
图 2. Meli 等 2025 原文 Figure 5,展示人类 FCD type 2b 皮层区域中 DRD1 和 DRD2 RNA puncta 在 control neurons、FCDIIB non-dysmorphic neurons 与 dysmorphic neurons 之间的差异 [2]。原文为 CC BY 4.0 开放获取。
图 2 说明。 A 部分是 DRD1/DRD2 FISH 与 SMI32、NeuN 标记的代表性图像。绿色 SMI32 标记 dysmorphic neurons,蓝色 NeuN 标记神经元,红色 puncta 对应 DRD1 或 DRD2 transcript。B 和 C 分别统计 pediatric patients 与 adult patients。儿童 FCD 标本中,NeuN SMI32-positive dysmorphic neurons 的 DRD1 和 DRD2 puncta/cell 明显高于 control neurons 和 FCDIIB 区域中的 non-dysmorphic neurons;成人样本中也能看到 dysmorphic neurons 的表达升高趋势,尤其在 pooled 或特定皮层区域分析中更明显。作者还检查了细胞体大小,认为这种受体表达升高不能简单解释为“细胞更大所以 puncta 更多”。
这个结果给出一个补偿性或重塑性的解释框架:当病灶区 DA 输入密度、层化分布或 varicosity 结构改变时,局部细胞可能通过改变 receptor transcript expression 来重设对 DA 信号的敏感性。但这种重设未必是有益补偿。D1-like 和 D2-like receptors 在皮层中会通过不同 G-protein 通路影响兴奋性、突触可塑性和网络状态;在本来已经发育异常、mTOR 活化、形态异常的 dysmorphic neurons 中,受体表达改变可能进一步放大网络不稳定性。
4. 把两篇文章放在一起:能量供应和调制输入都服务于“活动状态”
Kumar 等的脂滴论文强调 fuel flux:神经元可能持续把 triglyceride-derived fatty acids 从脂滴动员出来,经由线粒体氧化支持突触 ATP 供应 [1]。Meli 等的 FCD 论文强调 modulatory landscape:FCD type 2b 病灶中的 DA axonal innervation、varicosity distribution 和 DRD1/DRD2 expression 都可能偏离正常皮层 [2]。一个讲燃料,一个讲调制,但它们都指向同一个核心变量:局部神经网络如何维持和切换活动状态。
突触活动不是抽象的电信号。它需要囊泡循环、膜电位恢复、离子梯度维持、线粒体 ATP、局部代谢底物、受体状态和轴突输入共同支撑。癫痫发作也不是单纯“电太多”,而是局部网络在发育、代谢、调制和结构约束下进入异常同步状态。若脂滴燃料动员不足,突触末梢可能更难在高频活动后恢复;若 DA 输入和受体表达异常,病灶对状态调制信号的响应也会改变。二者都可能影响发作阈值,只是作用层级不同。
这也提示后续研究可以从三个方向推进。第一,在 FCD 或其他局灶性癫痫病灶中检测脂滴、DDHD2、CPT1、β-oxidation marker 和线粒体功能,看看病灶区是否存在局部燃料流异常。第二,把 DA/NE/5-HT 等 neuromodulatory axons 与代谢标记放在同一空间框架中分析,而不是分别研究“神经递质”和“代谢”。第三,在癫痫模型中同时记录活动状态、代谢状态和调制输入,区分哪些改变是发作前驱,哪些只是反复发作后的适应或损伤。
5. 一个更谨慎的结论
目前不能把这两篇论文直接连成因果链。脂滴燃料研究主要来自正常神经元、生化阻断和 DDHD2/CPT1 操作;FCD 多巴胺研究主要来自 FCD type 2b 标本和 mTOR hyperactivation 模型。它们的交叉点仍然是假设层面,而不是已经证明的机制链。但这个假设很有价值:局灶性癫痫病灶可能不是单一通路异常,而是局部细胞发育、轴突输入、受体表达和能量供应共同重排后的网络状态。
对读文献来说,这比寻找一个“主因”更有用。FCD 的结构异常解释了病灶的形成,多巴胺调制异常解释了病灶如何被状态信号调控,脂滴燃料通路则提醒我们高活动网络必须面对局部能量预算。真正需要关注的是这些层级如何耦合,以及哪一层最适合成为可干预的入口。
参考文献
- [1] Kumar M, Wu Y, Knapp J, Pontius CL, Park D, Witte RE, McAllister R, Gupta K, Rajagopalan KN, De Camilli P, Ryan TA. Triglycerides are an important fuel reserve for synapse function in the brain. Nature Metabolism. 2025;7(7):1392-1403. DOI: 10.1038/s42255-025-01321-x.
- [2] Meli N, Sheran K, Pitsch J, Krabbe S, Borger V, Baumgartner T, Becker A, Blaess S. Alterations in dopaminergic innervation and receptors in focal cortical dysplasia. Brain. 2025;148(8):2899-2911. DOI: 10.1093/brain/awaf080.